| Issue |
Cah. Agric.
Volume 34, 2025
|
|
|---|---|---|
| Article Number | 31 | |
| Number of page(s) | 9 | |
| DOI | https://doi.org/10.1051/cagri/2025031 | |
| Published online | 02 September 2025 | |
Article de synthèse / Review Article
Espèces végétales invasives : processus d’invasion et répercussions sur l’environnement, les services écosystémiques et la santé humaine
Invasive plant species: invasion processes and impacts on the environment, ecosystem services and human health
Université de Bourgogne Europe, Institut Agro Dijon, INRAE, UMR Agroécologie, Dijon, France
* Auteur de correspondance : This email address is being protected from spambots. You need JavaScript enabled to view it.
Résumé
Les invasions biologiques, phénomène naturel à l’origine mais amplifié par l’homme, deviennent écologiquement et économiquement préoccupantes. Elles s’inscrivent dans un continuum ponctué d’étapes (introduction-naturalisation-établissement-dispersion) déterminantes. Disposant d’une plasticité phénotypique et génotypique importante, les plantes invasives s’adaptent à de nombreuses conditions environnementales. Le réchauffement climatique, associé aux activités anthropiques (échanges internationaux, modification du paysage…), favorise leur progression. Malgré l’intérêt qui a prévalu à leur introduction, elles affectent fortement la biodiversité en excluant des plantes indigènes et le cortège faunistique associé, modifient le fonctionnement des biotopes envahis, affectent la santé des hommes et des animaux, et suscitent des coûts de gestion grandissant. Cette revue vise à sensibiliser l’opinion aux risques écologiques et sociétaux associés à la présence de plantes invasives dans les écosystèmes.
Abstract
Biological invasions, a natural phenomenon amplified by humans, are becoming an ecological and economic concern. They are part of a continuum punctuated by decisive stages (introduction-naturalization-establishment-dispersion). Thanks to significant phenotypic and genotypic plasticity, invasive plants adapt to many environmental conditions. Global warming associated with anthropogenic activities (international trade, landscape modification, etc.) favors their progression. Despite the interest that prevailed in their introduction, they strongly impact biodiversity by excluding native plants and the associated fauna, modify the functioning of invaded biotopes, affect the health of humans and animals, and generate increasing management costs. This review aims to raise awareness of the ecological and societal risks associated with the presence of invasive plants in ecosystems.
Mots clés : invasion biologique / continuum / adaptation / biodiversité / toxicité
Key words: biological invasion / continuum / adaptation / biodiversity / toxicity
© L. Pilet et al., Hosted by EDP Sciences 2025
 This is an Open Access article distributed under the terms of the Creative Commons Attribution License CC-BY-NC (https://creativecommons.org/licenses/by-nc/4.0), which permits unrestricted use, distribution, and reproduction in any medium, except for commercial purposes, provided the original work is properly cited.
This is an Open Access article distributed under the terms of the Creative Commons Attribution License CC-BY-NC (https://creativecommons.org/licenses/by-nc/4.0), which permits unrestricted use, distribution, and reproduction in any medium, except for commercial purposes, provided the original work is properly cited.
1 Introduction
Qu’elles concernent le monde microbien (Faillace et al., 2017), animal (Medlock et al., 2015) ou végétal (Vilà et al., 2024), les invasions biologiques sont écologiquement et économiquement préoccupantes (Bernery et al., 2021). Déjà évoquées comme un facteur participant à la conquête de niches nouvelles par Darwin (1859), les invasions biologiques sont aujourd’hui un phénomène mondial associé aux activités anthropiques. La domination humaine a été accompagnée par la redistribution des espèces au-delà des barrières géographiques les limitant à leur habitat d’origine (McNeely, 2004). Ces invasions s’accentuent en raison de la croissance du commerce mondial qui entraîne des opportunités accrues de redistribution et des conditions propices à la propagation d’organismes non indigènes (Henderson et al., 2006). Cependant, les incidences qu’ont ces organismes sur l’environnement diffèrent selon les espèces et les milieux colonisés (van Wilgen et al., 2022). Leur position dans les réseaux trophiques et leur capacité de colonisation interviennent sur la nature, l’intensité et l’ampleur des répercussions que ces organismes ont dans la zone envahie. Elles se distinguent par des effets écologiques (altération du biotope et atteinte à la biodiversité) (Vilà et Hulme, 2017), des effets sanitaires (nouveaux agents pathogènes) (Lühken et al., 2023) et des effets économiques incluant les coûts de gestion et les tentatives d’éradication (Boltovskoy et al., 2022). Trop peu d’articles scientifiques ou de vulgarisation rédigés en français font état des répercussions qu’ont les espèces invasives, notamment les plantes, sur notre environnement, alors que la littérature anglo-saxonne est particulièrement abondante dans ce domaine. Une analyse bibliométrique, réalisée le 13 mai 2025 sur la plateforme Web of Science™ et reposant sur la présence des mots clés « invasive plant » comme sujet d’étude des publications, révèle l’intérêt et la préoccupation grandissante suscités, notamment depuis 2000, par le nombre croissant de situations générées par des plantes invasives (Fig. 1). Parmi les 34 773 articles publiés durant cette période, dont seulement 56 en langue française, 2227 sont des articles de revue (sept en langue française) et 7830 associent les plantes invasives aux plantes adventices. Les thématiques dans lesquelles s’inscrivent ces publications relèvent essentiellement de l’écologie (11 664), des sciences du végétal (8004), de la biodiversité (4629), des sciences de l’environnement (5022), de l’agronomie et l’agriculture (2563), de la biologie évolutive (914) et des ressources en eau (512). L’objectif de la présente étude n’est pas de présenter une synthèse exhaustive de ces 34 773 publications, mais, via quelques exemples, de sensibiliser l’opinion aux risques (écologiques, sanitaires, économiques) associés aux plantes invasives dans notre environnement. L’approche suivie consiste à décrire les processus de l’invasion puis à donner les caractéristiques des espèces invasives d’une part et des milieux envahis d’autre part, en insistant sur les facteurs, notamment anthropiques, favorisant ces processus.
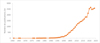 |
Fig. 1 Nombre annuel de publications scientifiques publiées sur la plateforme Web of Science™ de 1960 (date de la première publication) au 13 mai 2025 (date de consultation de la base de données) et portant sur les plantes invasives comme sujet d’étude (mots-clés utilisés pour l’analyse bibliométrique : « invasive plant »). Annual number of scientific publications published on the Web of Science™ platform from 1960 (date of first publication) to May 13, 2025 (date of database consultation) and relating to invasive plants as a subject of study (keywords used for bibliometric analysis: “invasive plant”). |
2 Processus d’invasion
Blackburn et al. (2011) ont proposé un cadre conceptuel intégrant les différentes étapes du processus, chacune constituant des barrières successives qui, selon qu’elles seront ou non franchies par la population concernée, aboutiront ou non à une invasion biologique (Fig. 2). Cette formalisation du processus permet de proposer des définitions des objets (individus, populations, espèces, quel que soit le règne), mécanismes (transport, introduction, captivité-culture-état sauvage) et fonctions (survie, reproduction, dispersion, mais aussi gestion, prévention, contrôle, éradication…) associés au franchissement des barrières. L’ensemble du processus introduction-naturalisation-établissement-dispersion a été qualifié de « continuum d’invasion » dans une revue dédiée à la naturalisation des plantes introduites par l’homme (Richardson et Pyšek, 2012).
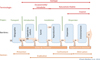 |
Fig. 2 Processus d’invasion biologique divisé en une série d’étapes ou barrières à surmonter pour qu’une espèce ou une population passe à l’étape suivante. A : Individus non transportés au-delà des limites de l’aire de répartition naturelle. B : Individus transportés au-delà des limites de leur aire de répartition naturelle. B1 : en captivité ou en quarantaine (mesures explicites de confinement). B2 : en culture (mesures pour limiter la dispersion). B3 : relâchés dans un nouvel environnement. C : Individus relâchés dans la nature dans le lieu d’introduction. C0 : mais incapables de survivre pendant une période significative. C1 : survivant mais pas de reproduction. C2 : survivant, reproduction en cours, mais population non autosuffisante. C3 : survivant, se reproduisant et population autonome. D : Population autosuffisante dans la nature, avec des individus survivant à une distance significative du point d’introduction d’origine. E : Espèce entièrement envahissante, dont les individus se dispersent, survivent et se reproduisent sur plusieurs sites dans un spectre plus ou moins grand d’habitats et d’étendues d’occurrence (d’après Blackburn et al., 2011). Biological invasion process divided into a series of stages or barriers that must be overcome for a species or population to move to the next stage. A: Individuals not transported beyond the limits of their natural range. B: Individuals transported beyond the limits of their natural range. B1: In captivity or quarantine (explicit containment measures). B2: In culture (measures to limit dispersal). B3: Released into a new environment. C: Individuals released into the wild at the point of introduction. C0: But unable to survive for a significant period. C1: Surviving but not reproducing. C2: Surviving, reproducing, but the population is not self-sustaining. C3: Surviving, reproducing, and self-sustaining. D: Self-sustaining population in the wild, with individuals surviving a significant distance from the point of introduction of origin. E: A fully invasive species, whose individuals disperse, survive, and reproduce across multiple sites within a more or less broad spectrum of habitats and ranges of occurrence (after Blackburn et al., 2011). |
2.1 Origine des introductions : un phénomène naturel amplifié par les activités humaines
Les naturalistes Charles Darwin (1809–1882) et Alfred Russel Wallace (1823–1913) avaient relevé au cours de leurs expéditions que les plantes et les animaux différaient d’un endroit à l’autre et que des modèles de répartition caractérisaient certaines zones de la planète. L’analyse des populations indigènes, de leur évolution et de leur adaptation aux conditions environnantes dans des milieux clos ou semi-clos les a conduits à des conclusions concordantes leur permettant de proposer, concurremment, la théorie de la sélection naturelle et la notion de biogéographie.
Les espèces possédant une grande plasticité phénotypique et génétique ont plus de chances de se disséminer (Rejmánek, 2000). La capacité de pression des propagules, un concept englobant la variation de la quantité, de la qualité, de la composition et du taux d’approvisionnement en propagules, influe sur la dispersion et la colonisation de l’espèce. La dissémination à partir du point d’origine dépend du mode de dispersion et des caractéristiques du milieu (Henderson et al., 2006). Le délai d’invasion peut être expliqué par une croissance lente dans les premiers stades avant une croissance exponentielle, des adaptations génotypiques, des perturbations cycliques ou de nouvelles adaptations au milieu (ensoleillement pour les espèces d’ombre par exemple) (Hobbs et Humphries, 1995). Des analyses phylogénétiques confortées par des analyses de fossiles révèlent que des migrations naturelles se sont produites au cours des millénaires, ce qui permet de savoir si une population est native ou issue de la colonisation plus ou moins ancienne dans une région donnée (Hill et Khan, 2023). Les facteurs climatiques et géologiques seraient associés à ces migrations, mais d’autres facteurs non encore expliqués pourraient également y contribuer. Ainsi, Darwin (1859) décrivait déjà la présence d’un chardon non natif invasif dans des régions peuplées d’aborigènes autarciques en Argentine et suggérait que ce chardon avait migré naturellement.
Depuis des millénaires, l’homme importe volontairement des espèces végétales pour des raisons alimentaires (maïs, tomate, pomme de terre…), ornementales ou esthétiques (bougainvillier, glycine de Chine, mimosa…), ou encore pour le besoin de pratiques culturales telles que la couverture des sols, la création de haies brise-vent, la production de biomasse ou pour le fourrage (Bell et al., 2003 ; Schnitzler et Essl, 2015). L’augmentation de la présence d’espèces invasives est due à l’intensification d’activités humaines comme l’agriculture, les échanges et les transports dans un contexte de mondialisation et d’explosion de la démographie (Driscoll et al., 2014). Actuellement, près de 14 000 espèces végétales exotiques naturalisées sont reportées à travers le monde avec notamment 5958 taxons en Amérique du Nord, 4139 en Europe et 3886 en Asie australe (van Kleunen et al., 2019).
L’introduction de plantes ornementales est la principale cause de la présence de plantes ligneuses invasives aux États-Unis, alors que l’introduction involontaire par le biais de sol ou de semences contaminées, de fourrage, de matériel agricole et de marchandises, est la plus fréquente cause de la présence de graminées et herbacées invasives (Chauvel et al., 2006 ; Goss et al., 2020). En Californie, parmi les 78 plantes les plus invasives, 41 ont été introduites comme plantes ornementales et huit pour contrôler l’érosion des sols (Bossard et al., 2000). Au Canada, 1229, soit 24 % des espèces végétales vasculaires, sont non natives et 486 de ces espèces sont invasives (Nguyen et al., 2021).
Certaines plantes invasives importées volontairement ont subi des sélections artificielles ou naturelles. Ces espèces, au départ sauvages, sont devenues cultivées puis invasives, alors que les plantes invasives importées involontairement sont souvent des espèces adaptées à l’environnement urbain ou agricole. Ce sont, en général, des plantes sauvages devenues adventices puis invasives (Goss et al., 2020). En France, de nombreuses plantes exotiques telles que la griffe de sorcière (Carpobrotus edulis), importée pour ses qualités de couvre-sol, le figuier de Barbarie (Opuntia ficus-indica) et l’agave d’Amérique (Agave americana), importés pour leurs qualités ornementales et comestibles, envahissent les calanques de Marseille. L’ailante (Ailanthus altissima), importé pour l’élevage du bombyx de l’ailante (Samia cynthia), s’installe en forêt de Fontainebleau (Motard, 2009). Les jussies (Ludwigia peploides et L. grandiflora) abondent dans les zones humides, mettent en danger les écosystèmes locaux et gênent la navigation. En 2020, 200 tonnes de plantes exotiques envahissantes ont été arrachées à Marseille (Perrier, 2020). En Polynésie française, 70 % de la surface de l’île de Tahiti sont envahis par Miconia calvescens DC., surnommé le cancer vert (Alves et al., 2010). L’herbe de la pampa (Cortaderia selloana) est devenue invasive en Europe (Liendo et al., 2023). L’ambroisie à feuilles d’armoise (Ambrosia artemisiifolia), extrêmement allergisante, et le datura stramoine (Datura stramonium), particulièrement toxique, colonisent l’ensemble du territoire français (Chauvel et al., 2006 ; Reboud, 2019).
2.2 Déterminisme de l’invasion
La dynamique d’invasion est régie par des facteurs intrinsèques et extrinsèques à l’espèce invasive, comme le nombre d’individus initialement introduits, les caractéristiques physiologiques et adaptatives de l’espèce envahissante, et la vulnérabilité de l’environnement à l’invasion (Lonsdale, 1999).
2.2.1 Caractéristiques intrinsèques aux espèces végétales invasives
Les caractéristiques intrinsèques sont d’ordre morphologique, biochimique, physiologique, structural, et phénologique. Elles déterminent l’adaptation de la plante à l’environnement et peuvent varier dans le temps (Gioria et al., 2023). Certaines, telles que les taux de germination et de croissance, le mode de reproduction, le succès reproductif et le taux de survie, sont liées à des traits héréditaires, de même que le potentiel évolutif, la capacité de compétition et de dispersion, la plasticité phénotypique, la tolérance et la résistance (Tab. 1) (Baker, 1974 ; Korpelainen et Pietiläinen, 2023). L’expression de ces caractéristiques est néanmoins soumise aux contraintes biotiques et abiotiques auxquelles la plante doit s’adapter.
Ces traits biologiques qui déterminent l’aire de répartition et favorisent l’invasion des plantes sont associés aux petits génomes. Plus tolérants aux stress environnementaux, ils facilitent l’adaptation des plantes à des conditions locales nouvelles grâce à des processus épigénétiques associés à une durée de génération courte (Pyšek et al., 2018 ; Mounger et al., 2021 ; Guo et al., 2024). Paradoxalement, la polyploïdie aussi peut augmenter le potentiel invasif des plantes introduites en modifiant le patrimoine génétique, facilitant la dispersion à longue distance, la propagation, et la compétition avec d’autres espèces en quelques générations (Moura et al., 2021 ; Pyšek et al., 2023). Les plantes utilisées pour usage économique combinent souvent une bonne réussite d’invasion et de naturalisation ainsi qu’une large aire de répartition (Guo et al., 2019 ; van Kleunen et al., 2020). Une fois établies, les plantes non natives peuvent soit intégrer la flore locale, soit dominer les communautés natives (Rejmánek, 2000). Leur compétitivité vis-à-vis des ressources disponibles pour les autres plantes est un véritable atout. De même, la production de métabolites secondaires par une plante invasive peut avoir un effet allélopathique facilitant son établissement (Kalisz et al., 2021). Les plantes indigènes se retrouvent démunies pour concurrencer des plantes exotiques avec lesquelles elles n’ont pas d’histoire co-évolutive. Ainsi le nombre de plantes exotiques dépasserait le nombre de plantes indigènes sur plus d’un quart des îles du monde (IPBES, 2019). Des plantes exotiques comme l’armoise de Chine (Artemisia verlotiorum), qui n’ont a priori pas d’ennemis naturels susceptibles de limiter leur population dans la zone d’introduction, dirigent totalement l’allocation des ressources vers leur établissement, la production de leur biomasse et de leurs semences, et la compétition trophique et/ou spatiale avec les espèces natives (Blossey et Notzold, 1995). Au cours du temps, les hybridations inter et intra-spécifiques génèrent des individus de mieux en mieux adaptés (Ellstrand et Schierenbeck, 2000). Des indicateurs tels que la taille du génome, le stade de développement ou la physiologie de la plante informent sur son caractère invasif. Ainsi, les plantes à semences de petite taille se disséminent plus facilement que celles à semences de grande taille, et les plantes polyploïdes sont plus envahissantes que les plantes diploïdes (Gioria et al., 2023).
Caractéristiques intrinsèques de l’envahisseur idéal (Baker, 1974).
Intrinsic characteristics of the ideal invader (Baker, 1974).
2.2.2 Caractéristiques liées à l’environnement envahi
L’environnement est source de stress pour les plantes. De nombreuses espèces invasives montrent une capacité d’adaptation et une tolérance au stress importantes. Le cerisier tardif (Prunus serotina) montre une grande rapidité de reproduction et de colonisation grâce à ses semences et à sa multiplication végétative. Il développe des stratégies lui permettant de végéter en attendant des conditions favorables et s’acclimate à tout type de sol (Forte et al., 2019). Les stress sont amplifiés par le changement climatique qui handicape les espèces cultivées et favorise les espèces invasives (González-Orenga et al., 2022). Les conditions climatiques influencent la dissémination des semences, la dynamique des populations, la durée des cycles de vie ainsi que la fréquence et l’intensité des maladies (Amare, 2016). La hausse des températures à l’échelle mondiale modifie la répartition géographique des zones climatiques et donc la répartition et l’abondance de nombreuses espèces. L’expansion des activités urbaines et l’évolution des activités agricoles augmentent la fragmentation des habitats (pertes de connectivité entre des îlots d’habitats) (Bacles et al., 2006). Ces modifications fragilisent des populations natives au bénéfice de populations exogènes qui s’installent, se développent et réduisent la diversité floristique de l’habitat colonisé (Qian et Guo, 2010).
2.2.3 Interactions biotiques au sein de l’environnement envahi
2.2.3.1 Interactions néfastes à la plante invasive
Dans leur nouvel environnement, les plantes invasives ou exogènes doivent faire face à des agresseurs potentiels tels que des microorganismes pathogènes. La spécificité d’agents pathogènes ayant co-évolué avec leurs plantes hôtes indigènes permet à la plante invasive de ne pas être affectée par leur présence. Par contre, des champignons comme Botrytis cinerea, Rhizoctonia solani et Sclerotinia sclerotiorum, ainsi que des bactéries comme Clavibacter michiganensis, Erwinia amylovora et Ralstonia solanacearum ont un large spectre d’hôtes, et peuvent constituer localement un obstacle à l’installation de plantes invasives. À l’inverse, il existe des sols naturellement capables d’inhiber des maladies d’origine tellurique (Steinberg et al., 2019). Ces sols constituent des zones favorables à l’installation de plantes exogènes (Maron et al., 2014). La résistance ou la tolérance biotique à l’invasion est liée à la diversité des communautés réceptrices, notamment leur richesse spécifique, et aux similarités et dissimilarités fonctionnelles ou phylogénétiques entre les plantes natives et non natives. Un écosystème avec une grande richesse spécifique sera plus résistant à l’invasion qu’un écosystème peu diversifié (Gioria et al., 2023). Les plantes invasives sont également confrontées à des menaces liées à la microfaune tellurique, dont les larves d’insectes ou les nématodes (Rutter et al., 2022). Paradoxalement, une plante adventice invasive telle que la renouée du Japon (Reynoutria japonica) peut être naturalisée grâce à ses propriétés nématicides (Cerevková et al., 2019).
À la surface du sol, les plantes invasives sont confrontées aux espèces animales herbivores. Elles souffrent cependant moins des herbivores que les plantes natives, probablement grâce à des défenses chimiques (Locken et Kelsey, 1987). Les herbivores généralistes sont capables de détoxifier les défenses de plantes natives avec lesquelles ils ont co-évolué pour s’en nourrir (Cornell et Hawkins, 2003), mais si les réactions de défense des plantes invasives reposent sur des métabolites secondaires qui leur sont inconnus, les herbivores peuvent être dépourvus du mécanisme de détoxification et dissuadés de consommer la plante (Jogesh et al., 2008). En revanche, certaines plantes exotiques plus faiblement invasives sont consommées par les herbivores, ces derniers devenant pour l’homme des auxiliaires utilisables dans une stratégie de biocontrôle (Carpenter et Cappuccino, 2005).
2.2.3.2 Interactions bénéfiques à la plante invasive
Le mode de dispersion des semences est important dans la colonisation du milieu et différents types d’organismes (oiseaux, insectes, micro- et macrofaune) sur ou sous la surface du sol participent à leur dissémination (Rejmánek, 1996). Outre les microorganismes éventuellement pathogènes présents dans l’environnement dans lequel la semence s’installe, il existe de nombreux microorganismes commensaux qui n’affectent pas l’installation de la plante, et d’autres, mutualistes, tels que les Plant Growth Promoting Rhizobacteria (PGPR) ou Fungi (PGPF) qui interagissent positivement avec la plante. Des interactions symbiotiques entre des plantes invasives telles que le quinquina rouge (Cinchona pubescens), le goyavier (Psidium guajava) ou la centaurée (Centaurea maculausa), et des champignons mycorhiziens à arbuscules indigènes ont été observées aux Galapagos et aux États-Unis (Carey et al., 2004). Ces associations symbiotiques favorisent la colonisation de l’écosystème par les plantes invasives (Maron et al., 2014).
3 Conséquences de la présence de plantes invasives sur un territoire
3.1 En quoi les plantes invasives perturbent-elles notre environnement ?
Les plantes et animaux invasifs sont la deuxième cause de diminution de biodiversité, juste après la destruction anthropique directe des habitats (Livingstone et al., 2020). Quarante pour cent des espèces menacées le sont à cause d’envahisseurs (Bell et al., 2003). Certaines plantes invasives ont un développement florissant qui entre en compétition avec celui des espèces natives pour l’espace, la lumière et les ressources telluriques (Gao et al., 2014). L’hypothèse selon laquelle la compétitivité des plantes invasives augmenterait après leur introduction a d’ailleurs été proposée pour expliquer leur succès invasif (Zhang et al., 2019). Cependant, les effets compétitifs des espèces exotiques et la réponse compétitive des espèces indigènes peuvent évoluer au cours du temps. À mesure que le caractère nouveau d’un envahisseur diminue, l’expérience éco-évolutive accumulée par les espèces résidentes peut à terme limiter le succès des invasions (Sheppard et Brendel 2021). Certaines espèces invasives forment des couverts denses (tapis herbacés, couvertures de lianes, fourrés, forêts monospécifiques) qui, comme Miconia calvescens en Nouvelle-Calédonie, étouffent la végétation naturelle, éliminent les plantes indigènes et endémiques et réduisent fortement la biodiversité (Alves et al., 2010). Cette modification de la biodiversité affecte le biotope et la biocénose qu’il héberge, aussi bien en milieu terrestre (dont les forêts) qu’en milieu aquatique. Le bon fonctionnement de l’écosystème et les fonctions écosystémiques comme le cycle des nutriments, la composition atmosphérique, l’hydrologie, la géomorphologie, la production primaire et la décomposition de la matière organique sont perturbés (Rai et Singh, 2020). Certaines espèces comme Prunus serotina, en forêt de Compiègne, affectent le fonctionnement de la forêt en modifiant le cycle de l’azote au détriment des plantes indigènes de l’écosystème. Ce dysfonctionnement favorise également l’érosion des sols en causant leur appauvrissement et leur assèchement, ce qui augmente les risques d’incendie et altère les processus de régulation naturelle (Bell et al., 2003). Cercle infernal, le dérèglement du fonctionnement de l’écosystème conduit à la fragmentation des habitats, à la diminution des populations natives, et favorise l’installation de plantes invasives. La mobilité des plantes invasives est d’autant plus importante que les milieux naturels ont subi des perturbations. Lorsque les habitats naturels sont détruits, pour construire une route par exemple, les plantes exotiques peuvent s’installer plus facilement grâce à leurs importantes capacités d’adaptation aux environnements hostiles, telles que leur stratégie de reproduction végétative ou sexuée, leur capacité à produire un important stock semencier dans le sol et leur rapidité de croissance.
Les plantes exogènes ayant une tolérance élevée aux stress hydrique et thermique ou liés à l’augmentation des teneurs en CO2 sont favorisées par le changement climatique (Bradley et al., 2010). Certaines zones sensibles, comme les zones montagneuses, sont soumises à une migration en altitude de la flore indigène au bénéfice de plantes invasives adaptées à des températures plus élevées. Le réchauffement climatique pourrait favoriser l’expansion d’Ambrosia artemisiifolia sur 27 à 100 % des surfaces d’Europe du Nord en 2100 (Rasmussen et al., 2017) et ainsi affecter des populations jusqu’à présent non sensibilisées aux allergies dont cette espèce est responsable.
3.2 La santé par les plantes ? Allergies, empoisonnements… quand les plantes rendent malades
Outre qu’elles perturbent les biocénoses, certaines espèces de plantes posent un réel problème sanitaire pour l’homme et les animaux du fait des substances toxiques qu’elles synthétisent (Lazzaro et al., 2018). Les plantes anémophiles peuvent produire un pollen allergisant, voire asthmatisant, en raison de protéines ou glycoprotéines immunologiquement néfastes. C’est le cas de Ambrosia artemisiifolia, A. altissima, Parthenium hysterophorus, et de plantes appartenant aux genres Acacia, Acer, Casuarina, Eucalyptus, Helianthus, Platanus et Xanthium (Chen et al., 2018 ; Rai et Singh, 2020). Parmi ces plantes, A. artemisiifolia produit un pollen très allergisant qui affecte 6 à 12 % de la population française exposée, mais aussi la population de la plupart des pays européens où elle s’est installée (Agnew et al., 2018). Cinq grains de pollen par mètre cube d’air peuvent provoquer des rhinites, conjonctivites, symptômes respiratoires, urticaires, eczémas. Cette allergie provoque de l’asthme dans 50 % des cas (Lazzaro et al., 2018). Un Observatoire des ambroisies a été créé en France en 2011 pour coordonner les actions de prévention et de lutte contre cette plante (FREDON, 2017). La berce du Caucase (Heracleum mantegazzianum, Sommier & Levier), introduite dans un jardin botanique en Angleterre comme curiosité végétale au début du XXe siècle, s’est propagée dans de nombreux pays européens et en Amérique du Nord. Sa sève contient une substance irritante, la furanocoumarine, qui provoque des brûlures graves appelées phytophotodermatites (Lazzaro et al., 2018). Le raisin d’Amérique (Phytolacca americana) a été introduit en Europe comme plante ornementale et dans les régions minières de Chine pour ses propriétés médicamenteuses et phytoremédiatrices (Yuan et al., 2017). Il produit un grand nombre de composés toxiques présents dans le foin et l’ensilage (Caloni et Cortinovis, 2015 ; Nan et al., 2024). Les propriétés de plantes hyperaccumulatrices de métaux rares délétères pour les cultures peuvent expliquer la présence de plantes phytoremédiatrices devenues invasives hors de leur biotope d’origine (Peng et al., 2008). Cependant, ces mêmes plantes sont toxiques pour l’homme et les animaux de par les métabolites qu’elles produisent. C’est le cas de la morelle noire (Solanum nigrum), originaire d’Asie du Sud-Est, devenue cosmopolite en Europe et en Amérique du Nord. Les nombreux métabolites qu’elle produit ont des propriétés médicamenteuses à faible dose, mais la consommation de ses baies provoque de sérieux troubles digestifs et neurologiques (Chen et al., 2022). Le datura (Datura stramonium), originaire du Mexique, se propage depuis plusieurs décennies de manière exponentielle sur le territoire français, entraînant une augmentation des cas recensés d’empoisonnement (Reboud, 2019 ; Abia et al., 2021). Introduite sans doute involontairement en Europe, la plante a pu s’installer en France pour son intérêt ornemental, mais également pour ses propriétés pharmaceutiques en dépit de sa grande toxicité qui peut entraîner coma et mort lors d’ingestions, même en faibles quantités (Gaire et Subedi, 2013).
4 Conclusion
Les activités anthropiques, les changements climatiques dont l’homme est partie prenante et les caractéristiques génétiques et physiologiques des plantes sont les plus importants facteurs d’invasion de plantes. Naturel à l’origine, ce phénomène a été amplifié par l’homme via des introductions volontaires ou involontaires. Insuffisamment maîtrisé, il menace à présent l’intégrité des écosystèmes, la biodiversité, la santé et le bien-être humain. Le problème des invasions par les plantes a donné lieu à de nombreuses études. La plupart d’entre elles se focalisent sur un cas particulier lié à une région, à une plante ou à une des étapes du continuum d’invasion, mais relativement peu d’entre elles ont une vision globale avec une perspective à court, moyen et surtout long terme de ce que pourraient être nos écosystèmes dans quelques décennies, incluant la production agricole et le bien-être des hommes et des animaux. Une telle approche nécessite l’intégration de compétences complémentaires en écologie, génétique, géographie, climatologie, économie, sciences humaines, philosophie et mathématique, pour proposer un modèle permettant d’envisager les scénarios les plus probables. Il s’agit là d’un réel challenge auquel des éléments de réponse sont apportés par Blackburn et al. (2011) et Richardson et Pyšek (2012). Au-delà de la prise en compte des facteurs biologiques incluant des activités anthropiques, le coût économique associé à ces invasions doit être intégré dans l’évaluation du rôle que peuvent jouer ces plantes dans nos modèles.
Remerciements
Les auteurs remercient la Région Bourgogne-Franche-Comté et le département Santé des Plantes et Environnement de l’INRAE pour le financement de la thèse Itinéraire Chercheurs Entrepreneurs de Lolita Pilet, dans le cadre de laquelle cette revue bibliographique a été réalisée.
Références
- Abia WA, Montgomery H, Nugent AP, Elliott CT. 2021. Tropane alkaloid contamination of agricultural commodities and food products in relation to consumer health: Learnings from the 2019 Uganda food aid outbreak. Comprehensive Reviews in Food Science and Food Safety 20: 501–525. https://doi.org/10.1111/1541-4337.12664. [Google Scholar]
- Agnew M, Banic I, Lake IR, Goodess C, Grossi CM, Jones NR, et al. 2018. Modifiable risk factors for common ragweed (Ambrosia artemisiifolia) allergy and disease in children: A case-control study. International Journal of Environmental Research and Public Health 15(7): 1339. https://doi.org/10.3390/ijerph15071339. [Google Scholar]
- Alves JL, Barreto RW, Pereira OL, Soares, DJ. 2010. Additions to the mycobiota of the invasive weed Miconia calvescens (Melastomataceae). Mycologia 102(1): 69–82. https://doi.org/10.3852/09-070. [Google Scholar]
- Amare T. 2016. Review on impact of climate change on weed and their management. American Journal of Biological and Environmental Statistics 2(3): 21–27. https://doi.org/10.11648/j.ajbes.20160203.12. [Google Scholar]
- Bacles CFE, Lowe AJ, Ennos RA. 2006. Effective seed dispersal across a fragmented landscape. Science 311(5751): 628. https://doi.org/10.1126/science.1121543. [Google Scholar]
- Baker HG. 1974. The evolution of weeds. Annual Review of Ecology, Evolution, and Systematics 5: 1–24. https://doi.org/10.1146/annurev.es.05.110174.000245. [Google Scholar]
- Bell CE, Wilen CA, Stanton AE. 2003. Invasive plants of horticultural origin. HortScience 38(1): 14–16. https://doi.org/10.21273/hortsci.38.1.14. [Google Scholar]
- Bernery C, Leroy B, Diagne C, Courchamp F. 2021. [2024/09/03]. 1288 milliards de dollars : chiffrer les dégâts causés par les invasions biologiques pour enfin agir. https://theconversation.com/1-288-milliards-de-dollars-chiffrer-les-degats-causes-par-les-invasions-biologiques-pour-enfin-agir-158204. [Google Scholar]
- Blackburn TM, Pyšek P, Bacher S, Carlton JT, Duncan RP, Jarošík V, et al. 2011. A proposed unified framework for biological invasions. Trends in Ecology and Evolution 26(7): 333–339. https://doi.org/10.1016/j.tree.2011.03.023. [Google Scholar]
- Blossey B, Notzold R. 1995. Evolution of increased competitive ability in invasive nonindigenous plants: A hypothesis. The Journal of Ecology 83(5): 887–889. https://doi.org/10.2307/2261425. [Google Scholar]
- Boltovskoy D, Guiaşu R, Burlakova L, Karatayev A, Schlaepfer MA, Correa N. 2022. Misleading estimates of economic impacts of biological invasions: Including the costs but not the benefits. Ambio 51(8): 1786–1799. https://doi.org/10.1007/s13280-022-01707-1. [Google Scholar]
- Bossard CC, Randall JM, Horshovsky MC. 2000. Invasive plants of Californiaʼs wildlands. Berkeley and Los Angeles: University of California Press, 360 p. [Google Scholar]
- Bradley BA, Blumenthal DM, Wilcove DS, Ziska LH. 2010. Predicting plant invasions in an era of global change. Trends in Ecology and Evolution 25(5): 310–318. https://doi.org/10.1016/j.tree.2009.12.003. [Google Scholar]
- Caloni F, Cortinovis C. 2015. Plants poisonous to horse Europe. Equine Veterinary Education 27(5): 269–274. https://doi.org/10.1111/eve.12274. [Google Scholar]
- Carey EV, Marler MJ, Callaway RM. 2004. Mycorrhizae transfer carbon from a native grass to an invasive weed: Evidence from stable isotopes and physiology. Plant Ecology 172: 133–141. https://doi.org/10.1023/B:VEGE.0000026031.14086.f1. [Google Scholar]
- Carpenter D, Cappuccino N. 2005. Herbivory, time since introduction and the invasiveness of exotic plants. Journal of Ecology 93(2): 315–321. https://doi.org/10.1111/j.1365-2745.2005.00973.x. [Google Scholar]
- Cerevková A, Bobuľská L, Miklisová D, Renčo M. 2019. A case study of soil food web components affected by Fallopia japonica (Polygonaceae) in three natural habitats in Central Europe. The Journal of Nematology 51(1): 1–16. https://doi.org/10.21307/jofnem-2019-042. [Google Scholar]
- Chauvel B, Dessaint F, Cardinal-Legrand C, Bretagnolle F. 2006. The historical spread of Ambrosia artemisiifolia L. in France from herbarium records. Journal of Biogeography 33: 665–673. https://doi.org/10.1111/j.1365-2699.2005.01401.x. [Google Scholar]
- Chen K-W., Marusciac L, Tamas PT, Valenta R, Panaitescu C. 2018. Ragweed pollen allergy: Burden, characteristics, and management of an imported allergen source in Europe. International Archives of Allergy and Immunology 176(3-4): 163–180. https://doi.org/10.1159/000487997. [Google Scholar]
- Chen X, Dai X, Liu Y, Yang Y, Yuan L, He X, et al. 2022. Solanum nigrum Linn.: An insight into current research on traditional uses, phytochemistry, and pharmacology. Frontiers in Pharmacology 13. https://doi.org/10.3389/fphar.2022.918071. [Google Scholar]
- Cornell HV, Hawkins BA. 2003. Herbivore responses to plant secondary compounds: A test of phytochemical coevolution theory. The American Naturalist 161(4): 507–522. https://doi.org/10.1086/368346. [Google Scholar]
- Darwin CR. 1859. On the origin of species by means of natural selection, or the preservation of favored races in the struggle for life. London (UK): John Murray, 602 p. https://doi.org/10.5962/bhl.title.68064. [Google Scholar]
- Driscoll DA, Catford JA, Barney JN, Hulme PE, Inderjit, Martin TG, et al. 2014. New pasture plants intensify invasive species risk. Proceedings of the National Academy of Sciences of the USA 111(46): 16622–16627. https://doi.org/10.1073/pnas.1409347111. [Google Scholar]
- Ellstrand NC, Schierenbeck KA. 2000. Hybridization as a stimulus for the evolution of invasiveness in plants? Proceedings of the National Academy of Sciences of the USA 97(13): 7043–7050. https://doi.org/10.1073/pnas.97.13.7043. [Google Scholar]
- Faillace CA, Lorusso NS, Duffy S. 2017. Overlooking the smallest matter: Viruses impact biological invasions. Ecology Letters 20: 524–538. https://doi.org/10.1111/ele.12742. [Google Scholar]
- Forte TGW, Brundu G, Celesti-Grapow L, Siniscalco C, Barni E. 2019. Prunus serotina in Italy: A challenging candidate for the national list of priority invasive alien species. Plant Biosystems 153(6): 900–904. https://doi.org/10.1080/11263504.2019.1666173. [Google Scholar]
- FREDON. 2017. Observatoire des ambroisies. [2024/09/03]. https://ambroisie-risque.info/observatoire-des-ambroisies. [Google Scholar]
- Gaire BP, Subedi L. 2013. A review on the pharmacological and toxicological aspects of Datura stramonium L. Journal of Integrative Medicine 11(2): 73–79. https://doi.org/10.3736/jintegrmed2013016. [Google Scholar]
- Gao Y, Yu HW, He WM. 2014. Soil space and nutrients differentially promote the growth and competitive advantages of two invasive plants. Journal of Plant Ecology 7(4): 396–402. https://doi.org/10.1093/jpe/rtt050. [Google Scholar]
- Gioria M, Hulme PE, Richardson DM, Pyšek P. 2023. Why are invasive plants successful? Annual Review of Plant Biology 74: 635–670. https://doi.org/10.1146/annurev-arplant-070522-071021. [CrossRef] [PubMed] [Google Scholar]
- González-Orenga S, Boscaiu M, Verdeguer M, Sánchez-Moreiras AM, González L, et al. 2022. Adaptability of invasive plants to climate change. AgroLife Scientific Journal 11(2): 58–65. https://doi.org/10.17930/AGL202227. [Google Scholar]
- Goss EM, Kendig AE, Adhikari A, Lane B, Kortessis N, Holt RD, et al. 2020. Disease in invasive plant populations. Annual Review of Phytopathology 58: 97–117. https://doi.org/10.1146/annurev-phyto-010820-012757. [Google Scholar]
- Guo K, Pyšek P, van Kleunen M, Kinlock NL, Lučanová M, Leitch IJ, et al. 2024. Plant invasion and naturalization are influenced by genome size, ecology and economic use globally. Nature Communications 15: 1330. https://doi.org/10.1038/s41467-024-45667-4. [Google Scholar]
- Guo W-Y., van Kleunen M, Pierce S, Dawson W, Essl F, Kreft H, et al. 2019. Domestic gardens play a dominant role in selecting alien species with adaptive strategies that facilitate naturalization. Global Ecology and Biogeography 28: 628–639. https://doi.org/10.1111/geb.12882. [Google Scholar]
- Henderson S, Dawson TP, Whittaker RJ. 2006. Progress in invasive plants research. Progress in Physical Geography Earth and Environment 30(1): 25–46. https://doi.org/10.1191/0309133306pp468ra. [Google Scholar]
- Hill RS, Khan R. 2023. Past climates and plant migration − the significance of the fossil record. New Phytologist 238: 2668–2684. https://doi.org/10.1111/nph.18867. [Google Scholar]
- Hobbs RJ, Humphries SE. 1995. An integrated approach to the ecology and management of plant invasions. Conservation Biology 9(4): 761–770. https://doi.org/10.1046/j.1523-1739.1995.09040761.x. [Google Scholar]
- IPBES. 2019. Summary for policymakers of the global assessment report on biodiversity and ecosystem services of the Intergovernmental Science-Policy Platform on Biodiversity and Ecosystem Services. In : Díaz S, Settele J, Brondízio ES, Ngo HT, Guèze M, Agard J, et al., eds. Bonn (Germany): IPBES secretariat, 56 p. [Google Scholar]
- Jogesh T, Carpenter D, Cappuccino N. 2008. Herbivory on invasive exotic plants and their non-invasive relatives. Biological Invasions 6: 797–804. https://doi.org/10.1007/s10530-008-9236-z. [Google Scholar]
- Kalisz S, Kivlin SN, Bialic-Murphy L. 2021. Allelopathy is pervasive in invasive plants. Biological Invasions 23: 367–371. https://doi.org/10.1007/s10530-020-02383-6. [Google Scholar]
- Korpelainen H, Pietiläinen M. 2023. What makes a good plant invader? Life 13(7): 1596. https://doi.org/10.3390/life13071596. [Google Scholar]
- Lazzaro L, Essl F, Lugliè A, Padedda BM, Pyšek P, Brundu G. 2018. Invasive alien plant impacts on human health and well-being. In : Mazza G, Tricarico E, eds. Invasive species and human health. Wallingford (UK): CABI, pp. 16–33. https://doi.org/10.1079/9781786390981.0016. [Google Scholar]
- Liendo D, Campos JA, Gandarillas A. 2023. Cortaderia selloana, an example of aggressive invaders that affect human health, yet to be included in binding international invasive catalogues. NeoBiota 89: 229–237. https://doi.org/10.3897/neobiota.89.110500. [Google Scholar]
- Livingstone SW, Isaac ME, Cadotte MW. 2020. Invasive dominance and resident diversity: Unpacking the impact of plant invasion on biodiversity and ecosystem function. Ecological Monographs 90(4): e01425. https://doi.org/10.1002/ecm.1425. [Google Scholar]
- Locken LJ, Kelsey RG. 1987. Cnicin concentrations in Centaurea maculosa, spotted knapweed. Biochemical Systematics and Ecology 15(2): 313–320. https://doi.org/10.1016/0305-1978(87)90005-6. [Google Scholar]
- Lonsdale WM. 1999. Global patterns of plant invasions and the concept of invasibility. Ecology 80(5): 1522–1536. https://doi.org/10.1890/0012-9658(1999)080[1522:GPOPIA]2.0.CO;2. [Google Scholar]
- Lühken R, Brattig N, Becker N. 2023. Introduction of invasive mosquito species into Europe and prospects for arbovirus transmission and vector control in an era of globalization. Infectious Diseases of Poverty 12: 109. https://doi.org/10.1186/s40249-023-01167-z. [Google Scholar]
- Maron JL, Klironomos J, Waller L, Callaway RM. 2014. Invasive plants escape from suppressive soil biota at regional scales. Journal of Ecology 102: 19–27. https://doi.org/10.1111/1365-2745.12172. [Google Scholar]
- McNeely JA. 2004. Strangers in our midst: The problem of invasive alien species. Environment: Science and Policy for Sustainable Development 46(6): 16–31. https://doi.org/10.1080/00139157.2004.10545159. [Google Scholar]
- Medlock JM, Hansford KM, Versteirt V, Cull B, Kampen H, Fontenille D, et al. 2015.An entomological review of invasive mosquitoes in Europe. Bulletin of Entomological Research 105(6): 637–663. https://doi.org/10.1017/S0007485315000103. [Google Scholar]
- Motard E. 2009. Étude de l’Ailante (Ailanthus altissima (Mill.) Swingle) comme exemple de plante invasive : risques pour la biodiversité de la forêt de Fontainebleau. PhD Thesis, 261 p. [Google Scholar]
- Mounger J, Ainouche ML, Bossdorf O, Cavé-Radet A, Li B, Parepa M, et al. 2021. Epigenetics and the success of invasive plants. Philosophical Transactions of the Royal Society B-Biological Sciences 376: 15. https://doi.org/10.1098/rstb.2020.0117. [Google Scholar]
- Moura RF, Queiroga D, Vilela E, Moraes AP. 2021. Polyploidy and high environmental tolerance increase the invasive success of plants. Journal of Plant Research 134: 105–114. https://doi.org/10.1007/s10265-020-01236-6. [Google Scholar]
- Nan Q, Li C, Li X, Zheng D, Li Z, Zhao L. 2024. Modeling the potential distribution patterns of the invasive plant species Phytolacca americana in China in response to climate change. Plants 13(8): 1082. https://doi.org/10.3390/plants13081082. [Google Scholar]
- Nguyen N-A., Eskelson BNI, Gergel SE, Murray T. 2021. The occurrence of invasive plant species differed significantly across three urban greenspace types of Metro Vancouver, Canada. Urban Forestry & Urban Greening 59: 126999. https://doi.org/10.1016/j.ufug.2021.126999. [Google Scholar]
- Peng K, Luo C, You W, Lian C, Li X, Shen Z. 2008. Manganese uptake and interactions with cadmium in the hyperaccumulator—Phytolacca Americana L. Journal of Hazardous Materials 154(1-3): 674–681. https://doi.org/10.1016/j.jhazmat.2007.10.080. [Google Scholar]
- Perrier A. 2020. [2024/09/27]. Le Frioul débarrassé de 200 tonnes de plantes exotiques envahissantes. https://www.marcelle.media/arrachage-plantes-exotique-marseille/. [Google Scholar]
- Pyšek P, Lucanová M, Dawson W, Essl F, Kreft H, Leitch IJ, et al. 2023. Small genome size and variation in ploidy levels support the naturalization of vascular plants but constrain their invasive spread. New Phytologist 239: 2389–2403. https://doi.org/10.1111/nph.19135. [Google Scholar]
- Pyšek P, Skálová H, Cuda J, Guo WY, Suda J, Dolezal J, et al. 2018. Small genome separates native and invasive populations in an ecologically important cosmopolitan grass. Ecology 99: 79–90. https://doi.org/10.1002/ecy.2068. [Google Scholar]
- Qian H, Guo Q. 2010. Linking biotic homogenization to habitat type, invasiveness and growth form of naturalized alien plants in North America. Diversity and Distributions 16(1): 119–125. https://doi.org/10.1111/j.1472-4642.2009.00627.x. [Google Scholar]
- Rai KP, Singh JS. 2020. Invasive alien plant species: Their impact on environment, ecosystem services and human health. Ecological Indicators 111: 106020. https://doi.org/10.1016/j.ecolind.2019.106020. [Google Scholar]
- Rasmussen K, Thyrring J, Muscarella R, Borchsenius F. 2017. Climate-change-induced range shifts of three allergenic ragweeds (Ambrosia L.) in Europe and their potential impact on human health. PeerJ 5: e3104. https://doi.org/10.7717/peerj.3104. [Google Scholar]
- Reboud X. 2019. Pourquoi et comment le datura contamine-t-il les denrées alimentaires ? In : The Conversation. https://theconversation.com/pourquoi-et-comment-le-datura-contamine-t-il-les-denrees-alimentaires-113772. [Google Scholar]
- Rejmánek M. 1996. A theory of seed plant invasiveness: The first sketch. Biological Conservation 78(1-2): 171–181. https://doi.org/10.1016/0006-3207(96)00026-2. [Google Scholar]
- Rejmánek M. 2000. Invasive plants: Approaches and predictions. Austral Ecology 25(5): 497–506. https://doi.org/10.1046/j.1442-9993.2000.01080.x. [Google Scholar]
- Richardson DM, Pyšek P. 2012. Naturalization of introduced plants: Ecological drivers of biogeographical patterns. New Phytologist 196(2): 383–396. https://doi.org/10.1111/j.1469-8137.2012.04292.x. [Google Scholar]
- Rutter WB, Franco J, Gleason C. 2022. Rooting out the mechanisms of root-knot nematode−plant interactions. Annual Review of Phytopathology 60: 43–76. https://doi.org/10.1146/annurev-phyto-021621-120943. [Google Scholar]
- Schnitzler A, Essl F. 2015. From horticulture and biofuel to invasion: The spread of Miscanthus taxa in the USA and Europe. Weed Research 55(3): 221–225. https://doi.org/10.1111/wre.12141. [Google Scholar]
- Sheppard CS, Brendel MR. 2021. Competitive ability of native and alien plants: Effects of residence time and invasion status. NeoBiota 47–69. https://doi.org/10.3897/neobiota.65.63179. [Google Scholar]
- Steinberg C, Edel-Hermann V, Alabouvette C, Lemanceau P. 2019. Soil suppressiveness to plant diseases. In : van Elsas JD, Trevors JT, Rosaldo AS, Nannipieri P, eds. Modern Soil Microbiology − Third Edition. New York (USA): CRC Press Taylor & Francis Group, pp. 345–361. [Google Scholar]
- van Kleunen M, Pyšek P, Dawson E, Essl F, Kreft H, Pergl J, et al. 2019. The Global Naturalized Alien Flora (GloNAF) database. Ecology 100(1): e02542. https://doi.org/10.1002/ecy.2542. [CrossRef] [PubMed] [Google Scholar]
- van Kleunen M, Xu X, Yang Q, Maurel N, Zhang Z, Dawson W, et al. 2020. Economic use of plants is key to their naturalization success. Nature Communications 11: 3201. https://doi.org/10.1038/s41467-020-16982-3. [Google Scholar]
- van Wilgen BW, Zengeya TA, Richardson DM. 2022. A review of the impacts of biological invasions in South Africa. Biological Invasions 24: 27–50. https://doi.org/10.1007/s10530-021-02623-3. [Google Scholar]
- Vilà M, Hulme PE. 2017. Impact of biological invasions on ecosystem services preface. Switzerland: Springer International Publishing, 259 p. https://doi.org/10.1007/978-3-319-45121-3. [Google Scholar]
- Vilà M, Trillo A, Castro-Díez P, Gallardo B, Bacher S. 2024. Field studies of the ecological impacts of invasive plants in Europe. NeoBiota 90: 139–159. https://doi.org/10.3897/neobiota.90.112368. [Google Scholar]
- Yuan M, Guo M-N., Liu W-S., Liu C, van Der Ent F A, Morel JL, et al. 2017. The accumulation and fractionation of rare earth elements in hydroponically grown Phytolacca americana L. Plant and Soil 421: 67–82. https://doi.org/10.1007/s11104-017-3426-3. [Google Scholar]
- Zhang ZJ, Zhou F, Pan XY, van Kleunen M, Liu M, Li B. 2019. Evolution of increased intraspecific competitive ability following introduction: The importance of relatedness among genotypes. Journal of Ecology 107: 387–395. https://doi.org/10.1111/1365-2745.13016. [Google Scholar]
Citation de l’article : Pilet L, Guillemin J-P, Edel-Hermann V, Steinberg C. 2025. Espèces végétales invasives : processus d’invasion et répercussions sur l’environnement, les services écosystémiques et la santé humaine. Cah. Agric. 34: 31. https://doi.org/10.1051/cagri/2025031
Liste des tableaux
Caractéristiques intrinsèques de l’envahisseur idéal (Baker, 1974).
Intrinsic characteristics of the ideal invader (Baker, 1974).
Liste des figures
 |
Fig. 1 Nombre annuel de publications scientifiques publiées sur la plateforme Web of Science™ de 1960 (date de la première publication) au 13 mai 2025 (date de consultation de la base de données) et portant sur les plantes invasives comme sujet d’étude (mots-clés utilisés pour l’analyse bibliométrique : « invasive plant »). Annual number of scientific publications published on the Web of Science™ platform from 1960 (date of first publication) to May 13, 2025 (date of database consultation) and relating to invasive plants as a subject of study (keywords used for bibliometric analysis: “invasive plant”). |
| Dans le texte | |
 |
Fig. 2 Processus d’invasion biologique divisé en une série d’étapes ou barrières à surmonter pour qu’une espèce ou une population passe à l’étape suivante. A : Individus non transportés au-delà des limites de l’aire de répartition naturelle. B : Individus transportés au-delà des limites de leur aire de répartition naturelle. B1 : en captivité ou en quarantaine (mesures explicites de confinement). B2 : en culture (mesures pour limiter la dispersion). B3 : relâchés dans un nouvel environnement. C : Individus relâchés dans la nature dans le lieu d’introduction. C0 : mais incapables de survivre pendant une période significative. C1 : survivant mais pas de reproduction. C2 : survivant, reproduction en cours, mais population non autosuffisante. C3 : survivant, se reproduisant et population autonome. D : Population autosuffisante dans la nature, avec des individus survivant à une distance significative du point d’introduction d’origine. E : Espèce entièrement envahissante, dont les individus se dispersent, survivent et se reproduisent sur plusieurs sites dans un spectre plus ou moins grand d’habitats et d’étendues d’occurrence (d’après Blackburn et al., 2011). Biological invasion process divided into a series of stages or barriers that must be overcome for a species or population to move to the next stage. A: Individuals not transported beyond the limits of their natural range. B: Individuals transported beyond the limits of their natural range. B1: In captivity or quarantine (explicit containment measures). B2: In culture (measures to limit dispersal). B3: Released into a new environment. C: Individuals released into the wild at the point of introduction. C0: But unable to survive for a significant period. C1: Surviving but not reproducing. C2: Surviving, reproducing, but the population is not self-sustaining. C3: Surviving, reproducing, and self-sustaining. D: Self-sustaining population in the wild, with individuals surviving a significant distance from the point of introduction of origin. E: A fully invasive species, whose individuals disperse, survive, and reproduce across multiple sites within a more or less broad spectrum of habitats and ranges of occurrence (after Blackburn et al., 2011). |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




